IF 12.4�!南京師范大學(xué)郭志剛/胡志剛教授團(tuán)隊(duì)發(fā)現(xiàn)APE1在HCC鐵死亡調(diào)控中的作用機(jī)制
肝細(xì)胞癌(HCC)是癌癥相關(guān)死亡的主要原因之一���,目前的治療措施仍不能有效改善HCC患者的總生存率。鐵死亡是由鐵依賴性脂質(zhì)過(guò)氧化引發(fā)的一種細(xì)胞死亡形式,已成為一種有前途的癌癥治療策略��,尤其是在HCC中��。然而�����,HCC中鐵死亡調(diào)節(jié)的機(jī)制尚不清楚����。2024年2月28日,南京師范大學(xué)郭志剛/胡志剛教授團(tuán)隊(duì)在Cell Death and Differentiation (IF 12.4)發(fā)表題為“APE1 inhibition enhances ferroptotic cell death and contributes to hepatocellular carcinoma therapy”的研究論文��。研究揭示了多功能酶APE1在鐵死亡調(diào)節(jié)中的新作用和機(jī)制����,并強(qiáng)調(diào)了靶向APE1作為HCC和其他癌癥治療策略的潛力�����。
本研究所用NRF2���、siAKT及siGSK3β質(zhì)粒�、APE1干擾慢病毒由維真助力提供�����!
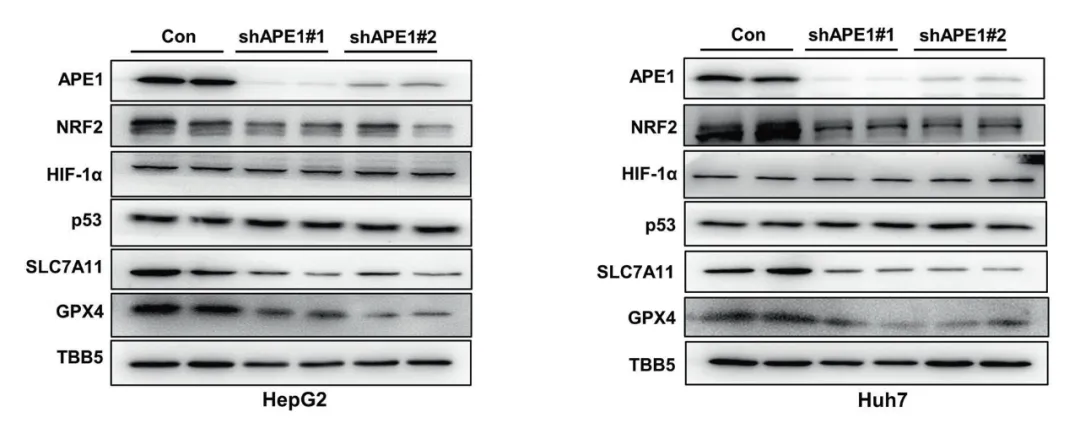
HCC細(xì)胞系中Lv-shAPE1的表達(dá)效果
研究結(jié)果
1、抑制APE1促進(jìn)HCC細(xì)胞鐵死亡
最近的多項(xiàng)研究表明鐵死亡與HCC的發(fā)展和治療反應(yīng)有關(guān),同時(shí)脫嘌呤/脫嘧啶核酸內(nèi)切酶1����,APE1在HCC中高水平表達(dá),促進(jìn)HCC的進(jìn)展并與其不良預(yù)后相關(guān),鑒于此�,作者探索了APE1是否參與HCC的鐵死亡�。首先�����,通過(guò)建立APE1敲低(APE1-KD)的HCC細(xì)胞系,發(fā)現(xiàn)APE1的沉默促進(jìn)了HCC細(xì)胞的鐵死亡�����,進(jìn)而檢測(cè)參與鐵死亡途徑關(guān)鍵基因的表達(dá),證實(shí)APE1通過(guò)NRF2/SLC7111/GPX4軸調(diào)節(jié)鐵死亡����。
接下來(lái)���,作者研究了APE1調(diào)節(jié)NRF2的具體機(jī)制����,發(fā)現(xiàn)APE1的敲低并不影響HCC細(xì)胞中NRF2的mRNA水平,而是影響其蛋白水平。抑制APE1顯著下調(diào)了糖原合成酶激酶-3β(GSK3β)的磷酸化水平,此外����,NRF2的泛素化水平在APE1-KD細(xì)胞中上調(diào),但在使用GSK3β抑制劑處理后得到逆轉(zhuǎn)����,表明APE1沉默通過(guò)GSK3β促進(jìn)NRF2泛素化。進(jìn)一步的分析表明APE1通過(guò)AKT影響GSK3β活性���,從而調(diào)節(jié)NRF2的穩(wěn)定性���,參與鐵死亡�����。
APE1通過(guò)NRF2/SLC7A11/GPX4軸調(diào)控鐵死亡
2���、APE1調(diào)節(jié)鐵死亡依賴于其氧化還原功能
通過(guò)在對(duì)照或APE1-KD HCC細(xì)胞中過(guò)表達(dá)或敲低NRF2,證實(shí)沉默APE1增強(qiáng)的鐵死亡依賴于NRF2�����。由于APE1同時(shí)具有DNA修復(fù)功能和氧化還原調(diào)節(jié)功能���,因此需明確具體哪種功能參與鐵死亡的調(diào)節(jié)�,數(shù)據(jù)顯示敲低APE1或使用CRT(APE1 DNA損傷修復(fù)功能抑制劑)增加了HCC細(xì)胞中的γ-H2AX(DNA損傷標(biāo)記物)水平�����,然而Ferr-1處理不影響APE1敲低細(xì)胞或CRT處理的細(xì)胞和對(duì)照細(xì)胞中的γ-H2AX水平,以及DNA損傷反應(yīng)信號(hào)水平;將CRT與erastin�����、RSL3聯(lián)合處理HCC細(xì)胞,發(fā)現(xiàn)CRT對(duì)erastin或RSL3誘導(dǎo)的HCC細(xì)胞鐵死亡沒(méi)有影響����,表明抑制APE1增強(qiáng)的鐵死亡與其DNA修復(fù)功能無(wú)關(guān)。隨后用E3330(APE1 氧化還原功能抑制劑)處理HCC細(xì)胞����,增強(qiáng)了erastin和RSL3誘導(dǎo)的細(xì)胞死亡�����,同時(shí)下調(diào)了HCC細(xì)胞中SLC7A11和GPX4的mRNA和蛋白水平����,以及NRF2的蛋白水平����。通過(guò)構(gòu)建APE1的DNA損傷修復(fù)功能突變體和氧化還原功能突變體,進(jìn)一步表明APE1通過(guò)其氧化還原功能調(diào)節(jié)GSK3β的磷酸化,從而影響NRF2的穩(wěn)定性�,并調(diào)節(jié)參與鐵死亡的SLC7A11和GPX4的表達(dá)。
APE1依靠其氧化還原功能參與鐵死亡
3��、抑制APE1增強(qiáng)了HCC對(duì)鐵死亡的敏感性
作者在裸鼠中建立了APE1-KD Huh7衍生的異種移植物模型�,以進(jìn)一步研究APE1抑制對(duì)體內(nèi)HCC鐵死亡的影響���。與對(duì)照組相比����,APE1-KD和erastin聯(lián)合處理提高了治療效果;通過(guò)流式細(xì)胞術(shù)檢測(cè)發(fā)現(xiàn)APE1的沉默上調(diào)了腫瘤組織中由erastin誘導(dǎo)的脂質(zhì)過(guò)氧化水平���。IHC染色和WB實(shí)驗(yàn)表明����,erastin處理增加了SLC7A11和CHAC1的蛋白質(zhì)水平,表明erastin對(duì)小鼠的治療是有效的����。此外�����,與野生型Huh7來(lái)源的腫瘤組織相比���,APE1-KD Huh7細(xì)胞來(lái)源的腫瘤細(xì)胞組織中的NRF2����、SLC7A11和GPX4蛋白水平降低�,并且APE1的敲低顯著上調(diào)了erastin誘導(dǎo)的4-HNE在腫瘤組織中的積累�。上述結(jié)果表明APE1缺失增強(qiáng)了erastin在體內(nèi)對(duì)HCC的治療作用。
沉默APE1增強(qiáng)HCC對(duì)體內(nèi)鐵死亡的敏感性
結(jié)論
研究表明抑制APE1可促進(jìn)HCC細(xì)胞中的鐵死亡��,揭示了APE1在調(diào)節(jié)肝癌細(xì)胞鐵死亡中的重要作用和具體機(jī)制,為肝細(xì)胞癌的治療提供了新靶點(diǎn)和新思路��。