骨關(guān)節(jié)炎治療新靶標(biāo)|祝文濤教授團(tuán)隊(duì)闡明mtDNA-IRF1-ZBP1-RIPK1是參與軟骨細(xì)胞損傷的病理軸
骨關(guān)節(jié)炎(OA)是最常見的退行性疾病之一,影響全球5億多人�����。關(guān)節(jié)軟骨的破壞是OA最基本的病理特征����,而軟骨細(xì)胞是關(guān)節(jié)軟骨中的主要細(xì)胞類型�����,控制著軟骨的完整性和穩(wěn)態(tài)�。目前���,OA軟骨細(xì)胞損傷和OA發(fā)病的分子機(jī)制在很大程度上仍有待闡明�。Z-DNA結(jié)合蛋白1(ZBP1)是一種參與多種炎癥性疾病的核酸傳感器��,但它是否以及如何導(dǎo)致OA尚不清楚���。
2024年7月18日,華中科技大學(xué)同濟(jì)醫(yī)學(xué)院附屬同濟(jì)醫(yī)院祝文濤教授團(tuán)隊(duì)在Cell Communication and Signaling (IF 8.2) 上發(fā)文“IRF1 regulation of ZBP1 links mitochondrial DNA and chondrocyte damage in osteoarthritis”,研究發(fā)現(xiàn)ZBP1表達(dá)與OA進(jìn)展呈正相關(guān)�,mtDNA-IRF1-ZBP1-RIPK1是參與軟骨細(xì)胞損傷的病理軸,抑制該軸可能是治療OA的可行方法���。

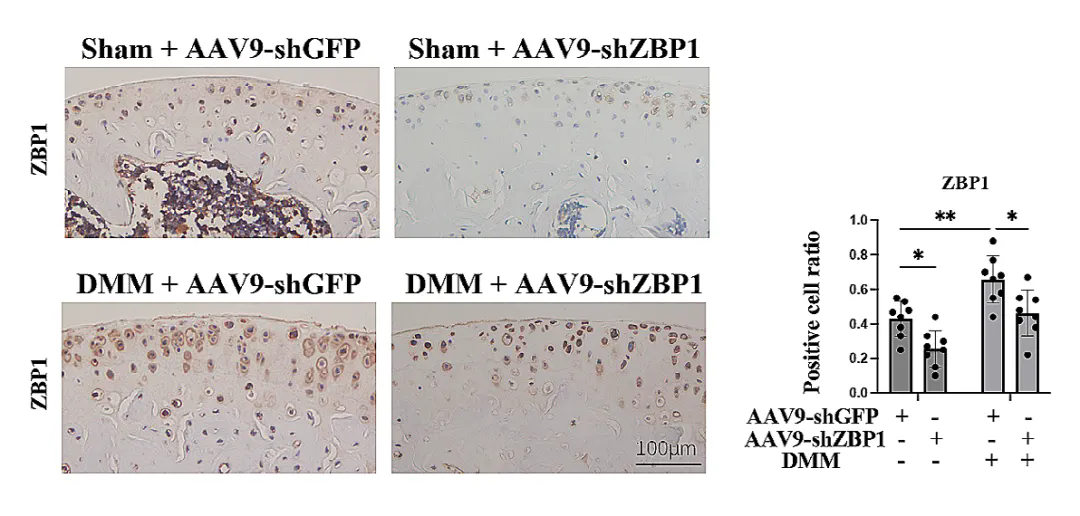
IHC染色顯示AAV9-shZBP1有效減少了ZBP1陽性細(xì)胞數(shù)量
研究結(jié)果
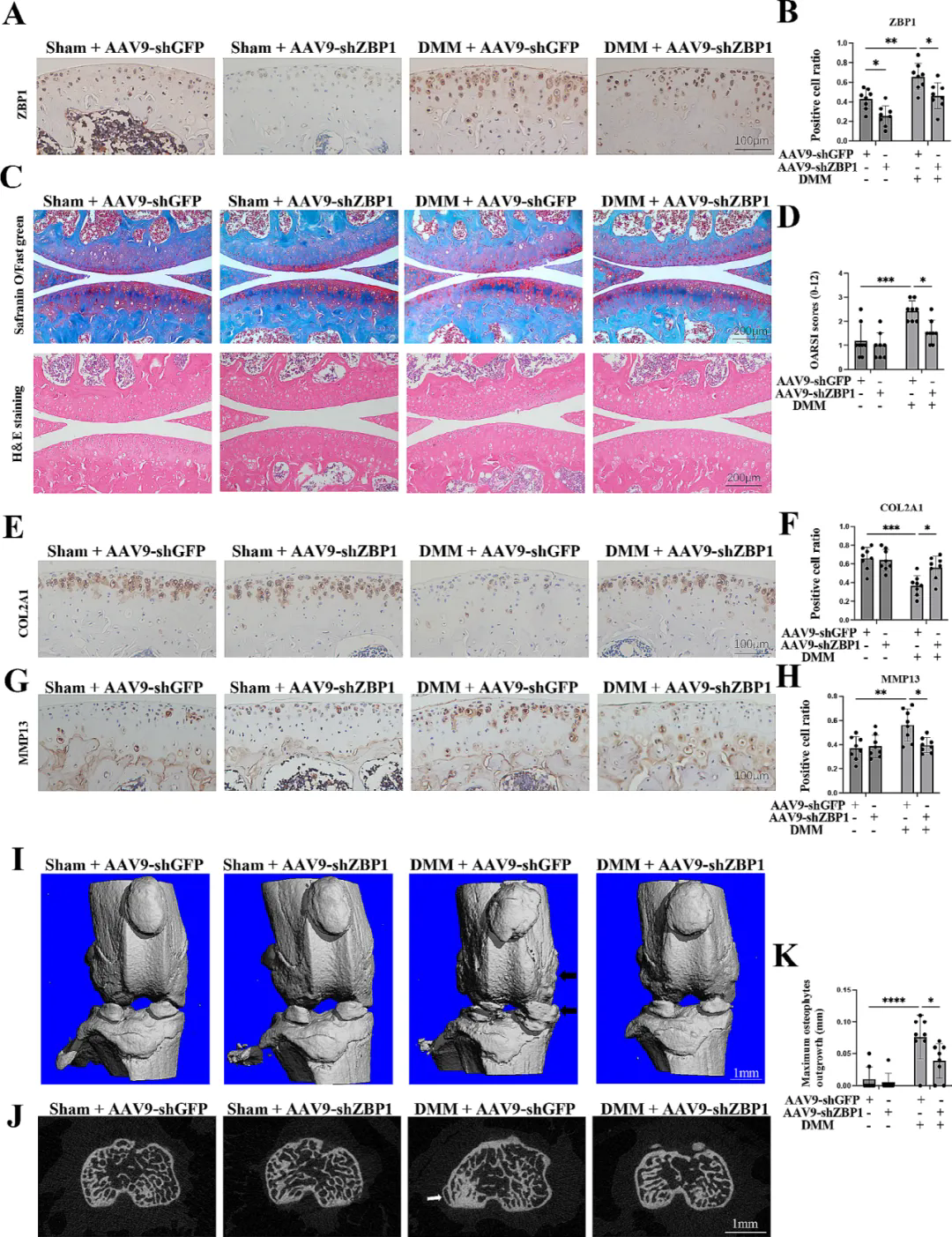
1��、AAV9-shZBP1敲低保護(hù)小鼠免受DMM誘導(dǎo)的軟骨退化和骨贅形成
OA樣本和創(chuàng)傷后OA小鼠模型中ZBP1的表達(dá)水平上調(diào)���,表明ZBP1表達(dá)與OA進(jìn)展密切相關(guān)�。為驗(yàn)證軟骨細(xì)胞中ZBP1的缺失是否能保護(hù)小鼠免受OA的侵害�,研究團(tuán)隊(duì)將AAV9-shZBP1注射到小鼠膝關(guān)節(jié)腔內(nèi),IHC結(jié)果證實(shí)���,與AAV9-shGFP組相比,AAV9-shZBP1有效地減少了ZBP1軟骨細(xì)胞的數(shù)量��。在首次注射AAV9兩周后���,進(jìn)行DMM手術(shù)或假手術(shù),并在術(shù)后第56天處死小鼠。與DMM組相比�,AAV9-shZBP1組小鼠關(guān)節(jié)軟骨退化較少��,OARSI評分較低�����。通過評估軟骨下骨和骨贅的變化�,發(fā)現(xiàn)接受DMM手術(shù)的AAV9-shZBP1注射小鼠骨贅形成減少,骨贅評分降低。上述結(jié)果表明,軟骨中ZBP1的下調(diào)保護(hù)了小鼠免受DMM誘導(dǎo)的軟骨退化和骨贅形成的影響��。
ZBP1對DMM小鼠的OA進(jìn)展至關(guān)重要
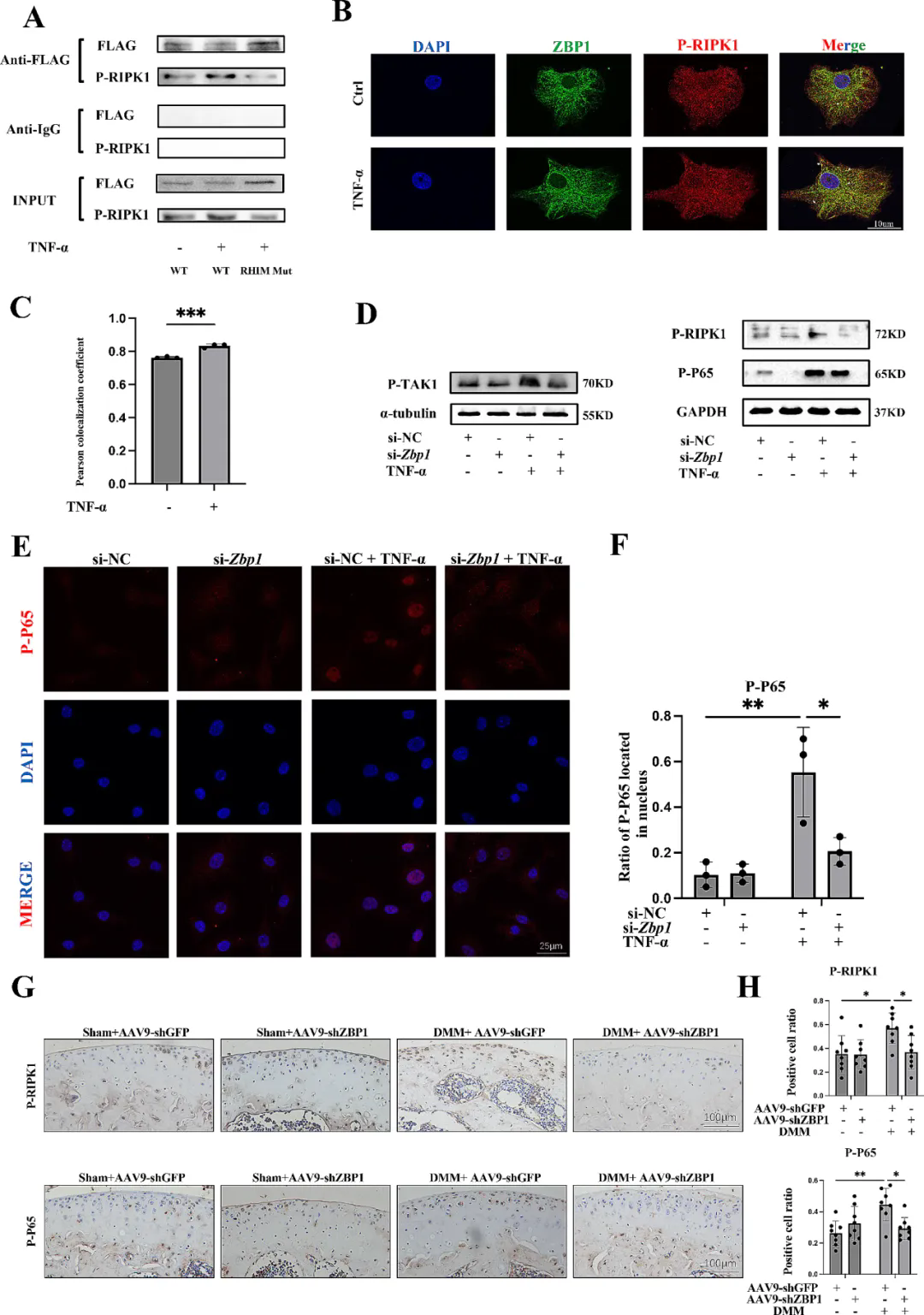
2����、ZBP1與RIPK1相互作用�,通過NF-κB信號通路促進(jìn)軟骨細(xì)胞損傷
由于ZBP1含有RIP同型相互作用基序(RHIM)�����,ZBP1與其他含RHIM的蛋白質(zhì)的相互作用是ZBP1信號轉(zhuǎn)導(dǎo)的基礎(chǔ)�,之前的研究表明了RIPK1-NF-κB信號通路在炎性軟骨細(xì)胞中的病理作用�����,因此研究團(tuán)隊(duì)分析了ZBP1和RIPK1在軟骨細(xì)胞中的相互作用�。IF共定位結(jié)果顯示�����,在TNF-α處理的軟骨細(xì)胞中���,ZBP1與P-RIPK1的共定位增加,與TNF-α組相比,ZBP1敲低降低了TAK1、P65和RIPK1的磷酸化���;IHC結(jié)果顯示,與DMM組相比�����,AAV9-shZBP1還降低了關(guān)節(jié)軟骨中P-P65和P-RIPK1的表達(dá)水平,表明ZBP1可以與RIPK1相互作用以激活RIPK1-TAK1-NF-κB信號通路,介導(dǎo)軟骨細(xì)胞炎癥和ECM降解���。進(jìn)一步研究證明ZBP1的表達(dá)受IRF1的調(diào)節(jié)����,過表達(dá)ZBP1逆轉(zhuǎn)了IRF1敲低對軟骨細(xì)胞的保護(hù)作用。
ZBP1與RIPK1相互作用����,激活TAK1-NF-κB通路
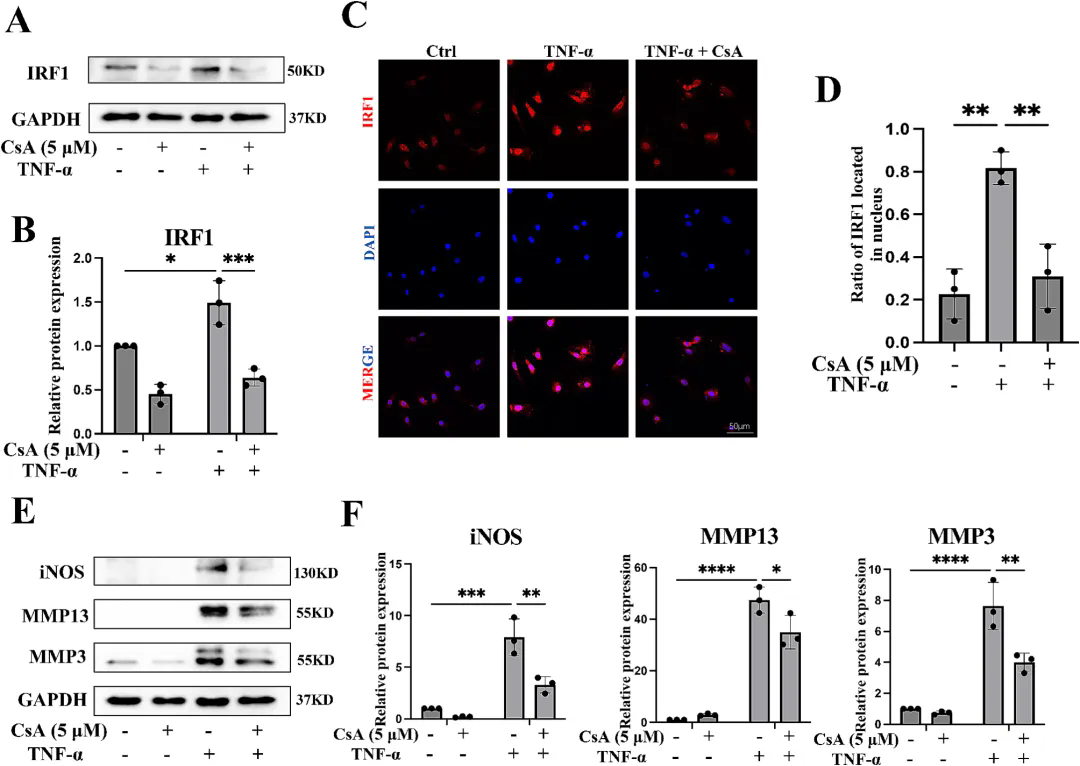
3�����、CsA治療抑制ZBP1��,減輕軟骨細(xì)胞損傷
由于在細(xì)胞應(yīng)激和線粒體功能障礙的條件下,mtDNA可以釋放到細(xì)胞質(zhì)或細(xì)胞外空間,與包括ZBP1在內(nèi)的模式識別受體結(jié)合,因此研究團(tuán)隊(duì)進(jìn)一步探討了OA軟骨細(xì)胞釋放的mtDNA是否調(diào)節(jié)ZBP1���。研究發(fā)現(xiàn)�����,TNF-α導(dǎo)致線粒體釋放更多的dsDNA�����,增加ZBP1和dsDNA的共定位��,而CsA(線粒體通透性轉(zhuǎn)換孔抑制劑)治療不僅降低了細(xì)胞質(zhì)中的mtDNA水平以及ZBP1和dsDNA的結(jié)合�,還降低了ZBP1��、p-RIPK1的表達(dá)水平�,表明CsA可以抑制mtDNA-ZBP1-RIPK1軸�。先前的研究證實(shí)IRFs可能受到mtDNA的調(diào)控����,檢測發(fā)現(xiàn)CsA降低了TNF-α處理的軟骨細(xì)胞中核IRF1的比例,顯著減輕了軟骨細(xì)胞的炎癥反應(yīng)和ECM降解�����,表明mtDNA可能在ZBP1的活性和表達(dá)中發(fā)揮雙重作用�����,導(dǎo)致軟骨細(xì)胞損傷�,CsA抑制mtDNA的釋放可以防止TNF-α誘導(dǎo)的軟骨細(xì)胞損傷���。
mtDNA對IRF1和軟骨細(xì)胞損傷的影響
結(jié)論
本研究揭示了ZBP1表達(dá)與OA之間的正相關(guān)關(guān)系�����,mtDNA-IRF1-ZBP1-RIPK1是參與軟骨細(xì)胞損傷的病理軸�����。此外�,CsA抑制mtDNA-IRF1-ZBP1軸可保護(hù)小鼠免受DMM誘導(dǎo)的OA進(jìn)展。研究結(jié)果強(qiáng)調(diào)了ZBP1在連接mtDNA和軟骨細(xì)胞損傷中的重要作用���,并揭示了一個(gè)可能用作OA治療靶點(diǎn)的新軸�����。